


 الفيزياء الكلاسيكية
الفيزياء الكلاسيكية
 الكهربائية والمغناطيسية
الكهربائية والمغناطيسية
 علم البصريات
علم البصريات
 الفيزياء الحديثة
الفيزياء الحديثة
 النظرية النسبية
النظرية النسبية
 الفيزياء النووية
الفيزياء النووية
 فيزياء الحالة الصلبة
فيزياء الحالة الصلبة
 الليزر
الليزر
 علم الفلك
علم الفلك
 المجموعة الشمسية
المجموعة الشمسية
 الطاقة البديلة
الطاقة البديلة
 الفيزياء والعلوم الأخرى
الفيزياء والعلوم الأخرى
 مواضيع عامة في الفيزياء
مواضيع عامة في الفيزياء|
أقرأ أيضاً
التاريخ: 20-5-2017
التاريخ: 2023-09-17
التاريخ: 2023-09-25
التاريخ: 2023-09-26
|
تتكون البلورات الأيونية من أيونات سالبة وأخرى موجبة. ويتم ترتيب الأيونات بحيث يكون تجاذب الأيونات مختلفة الشحنة أقوى من تنافر الأيونات متشابهة الشحنة. والرابطة الأيونية هي ما ينشأ عن التفاعل الكهروستاتيكي بين الأيونات مختلفة الشحنة ومن أشهر أمثلة هذه البلورات كلوريد الصوديوم وكلوريد السيزيوم اللذان جاء ذكرهما من قبل.
ويمكننا – على وجه العموم – اعتبار كل الأيونات داخل بلورة مكعبية بسيطة بأنها ذات قشرات إلكترونية مغلقة (مكتملة) كما في ذرات الغازات الخاملة. وعلى ذلك تكون الذرات المتعادلة في حالة فلوريد الليثيوم LiF – مثلا – ذات هيئة إلكترونية على النحو التالي:
F: 1s2 2s2 2p5
Li: 1s2 2s
أما الأيونان وحيدا الشحنة فيكونان كما يلي:
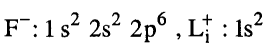
وهما في هذه الحالة شبيهان بذرتي الهليوم والنيون على الترتيب.
علينا – إذن – أن نتوقع توزيعا كروي التماثل للشحنة حول كل أيون في بلورة أيونية، وقد يكون هناك بعض التشوه في منطقة تماس الذرات المتجاورة، كما تأكد من دراسات الأشعة السينية للتوزيع الإلكتروني (الشكل 7-9).

شكل (7-9)
توزيع كثافة الإلكترونات في المستوى القاعدي لبلورة كلوريد الصوديوم



|
|
|
|
علامات بسيطة في جسدك قد تنذر بمرض "قاتل"
|
|
|
|
|
|
|
أول صور ثلاثية الأبعاد للغدة الزعترية البشرية
|
|
|
|
|
|
|
العتبة الحسينية تطلق فعاليات المخيم القرآني الثالث في جامعة البصرة
|
|
|