
تاريخ الفيزياء

علماء الفيزياء


الفيزياء الكلاسيكية

الميكانيك

الديناميكا الحرارية


الكهربائية والمغناطيسية

الكهربائية

المغناطيسية

الكهرومغناطيسية


علم البصريات

تاريخ علم البصريات

الضوء

مواضيع عامة في علم البصريات

الصوت


الفيزياء الحديثة


النظرية النسبية

النظرية النسبية الخاصة

النظرية النسبية العامة

مواضيع عامة في النظرية النسبية

ميكانيكا الكم

الفيزياء الذرية

الفيزياء الجزيئية


الفيزياء النووية

مواضيع عامة في الفيزياء النووية

النشاط الاشعاعي


فيزياء الحالة الصلبة

الموصلات

أشباه الموصلات

العوازل

مواضيع عامة في الفيزياء الصلبة

فيزياء الجوامد


الليزر

أنواع الليزر

بعض تطبيقات الليزر

مواضيع عامة في الليزر


علم الفلك

تاريخ وعلماء علم الفلك

الثقوب السوداء


المجموعة الشمسية

الشمس

كوكب عطارد

كوكب الزهرة

كوكب الأرض

كوكب المريخ

كوكب المشتري

كوكب زحل

كوكب أورانوس

كوكب نبتون

كوكب بلوتو

القمر

كواكب ومواضيع اخرى

مواضيع عامة في علم الفلك

النجوم

البلازما

الألكترونيات

خواص المادة


الطاقة البديلة

الطاقة الشمسية

مواضيع عامة في الطاقة البديلة

المد والجزر

فيزياء الجسيمات


الفيزياء والعلوم الأخرى

الفيزياء الكيميائية

الفيزياء الرياضية

الفيزياء الحيوية

الفيزياء والفلسفة

الفيزياء العامة


مواضيع عامة في الفيزياء

تجارب فيزيائية

مصطلحات وتعاريف فيزيائية

وحدات القياس الفيزيائية

طرائف الفيزياء

مواضيع اخرى
العملية ثابتة درجة الحرارة ( الأيسوثرمية)
المؤلف:
فريدريك بوش ، دافيد جيرد
المصدر:
اساسيات الفيزياء
الجزء والصفحة:
ص 451
30-6-2016
5494
العملية ثابتة درجة الحرارة ( الأيسوثرمية)
يقال أن العملية ايسوثرمية إذا تغيرت حالة النظام عند ثبوت درجة حرارته* وحيث أن الطاقة الداخلية تعتمد على درجة الحرارة فقط، إذن U = 0Δ أثناء العملية الأيسوثرمية. وفي هذه الحالة يتحول القانون الأول إلى الصورة:
(1) Q = W (للعملية الأيسوثرمية)
وهكذا فإن كل الحرارة المضافة تستهلك في بذل الشغل أثناء التمدد الأيسوثرمي . والعكس صحيح أيضاً ، فإن الشغل المبذول على الغاز أثناء الانضغاط الأيسوثرمي سوف يفقد كحرارة إلى الوسط المحيط. ويمثل الشكل 1) أ) وعاء يحتوي على كمية من غاز مثالي في حالة تلامس حراري جيد مع خزان حراري (فرن أو حمام تبريد أو جهاز آخر يمكنه أن يمد الغاز بالحرارة أو يستقبلها منه مع بقاء درجة حرارته ثابتة). فإذا وضعت الأثقال ببطء شديد على الكباس سوف يزداد ضغط الغاز ويقل حجمه ببطء شديد.
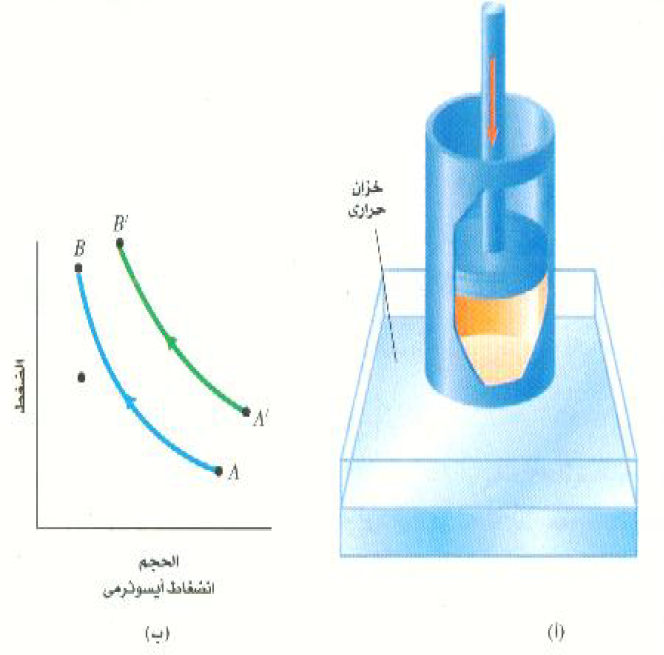
الشكل 1)): الرسم البياني PV لانضغاط أيسوثرمي. الأيسوثرمي A' B' يمثل العلاقة بين الضغط والحجم عند درجة حرارة أعلى من AB. لماذا؟
وحيث أن قانون الغاز المثالي ينص على أن حاصل الضرب PV يساوي مقداراً ثابتاً عند ثبوت درجة الحرارة، فإن هذا يعني بالتالي أن P يتناسب عكسياً مع V أثناء العملية الأيسوثرمية:
PV = constant
أو:
(2) 
هذه المعادلة تعطينا مسار العملية الأيسوثرمية ( والذي يسمى أيسوثرم) في الرسم البياني PV، والموضح بالشكل (1 ب). ويجب أن يلاحظ هنا أنه كلما ارتفعت درجة حرارة الأيسوثرم، كلما بعد موضعه بالنسبة إلى محوري الإحداثيات، فالأيسوثرم الأخضر AB في الشكل 1) ب) يمثل درجة حرارة أعلى من الأيسوثرم الأزرق AB.
من الممكن اشتقاق تعبير للشغل المبذول أثناء العملية الأيسوثرمية باستخدام طرق حساب التفاضل والتكامل. ونظراً لأن اشتقاق هذه العلاقة فوق المستوى الرياضي المطلوب لهذا المقرر، فإننا سنكتب النتيجة النهائية هنا بدون برهان:

حيث T هي درجة الحرارة المطلقة للأيسوثرم، Vf و Vi هما الحجمان النهائي والابتدائي للغاز؛ أما الدالة In فتمثل اللوغاريتم الطبيعي). ويلاحظ أن هذا التعبير الرياضي يعطي الشغل بالإشارة الصحيحة. ذلك أن ln أي عدد أصغر من 1 يكون سالباً، وهذه هي حالة انضغاط الغاز، حيث Vf < Vi.
___________________________
(*) عند رسم المنحني PV يفترض أن التغيرات التي تحدث في النظام بطيئة بدرجة كافية لكي يكون الضغط ودرجة الحرارة منتظمين في كل أجزاء النظام عند أية لحظة.
 الاكثر قراءة في الديناميكا الحرارية
الاكثر قراءة في الديناميكا الحرارية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















