
تاريخ الفيزياء

علماء الفيزياء


الفيزياء الكلاسيكية

الميكانيك

الديناميكا الحرارية


الكهربائية والمغناطيسية

الكهربائية

المغناطيسية

الكهرومغناطيسية


علم البصريات

تاريخ علم البصريات

الضوء

مواضيع عامة في علم البصريات

الصوت


الفيزياء الحديثة


النظرية النسبية

النظرية النسبية الخاصة

النظرية النسبية العامة

مواضيع عامة في النظرية النسبية

ميكانيكا الكم

الفيزياء الذرية

الفيزياء الجزيئية


الفيزياء النووية

مواضيع عامة في الفيزياء النووية

النشاط الاشعاعي


فيزياء الحالة الصلبة

الموصلات

أشباه الموصلات

العوازل

مواضيع عامة في الفيزياء الصلبة

فيزياء الجوامد


الليزر

أنواع الليزر

بعض تطبيقات الليزر

مواضيع عامة في الليزر


علم الفلك

تاريخ وعلماء علم الفلك

الثقوب السوداء


المجموعة الشمسية

الشمس

كوكب عطارد

كوكب الزهرة

كوكب الأرض

كوكب المريخ

كوكب المشتري

كوكب زحل

كوكب أورانوس

كوكب نبتون

كوكب بلوتو

القمر

كواكب ومواضيع اخرى

مواضيع عامة في علم الفلك

النجوم

البلازما

الألكترونيات

خواص المادة


الطاقة البديلة

الطاقة الشمسية

مواضيع عامة في الطاقة البديلة

المد والجزر

فيزياء الجسيمات


الفيزياء والعلوم الأخرى

الفيزياء الكيميائية

الفيزياء الرياضية

الفيزياء الحيوية

الفيزياء والفلسفة

الفيزياء العامة


مواضيع عامة في الفيزياء

تجارب فيزيائية

مصطلحات وتعاريف فيزيائية

وحدات القياس الفيزيائية

طرائف الفيزياء

مواضيع اخرى
التماثل الجزيئي Molecular Symmetry
المؤلف:
الدكتور صلاح الدين محمود يونس
المصدر:
الفيزياء الجزيئية
الجزء والصفحة:
ص 17
25-9-2020
8666
التماثل الجزيئي Molecular Symmetry
التماثل خاصية تعتمد على تركيب الجزيئة فبعض الجزيئات تملك تماثلا تركيبيا وبعضها الاخر لا يملك ذلك ودراسة خواص تماثل الجزيئات فرع مهم في الفيزياء الجزيئية لانها تقود الى استخلاص معلومات عن تركيب الجزيئة فكلما امتلكت الجزيئة تماثلا اكبر يصبح من الاسهل تعيين اعلومات الجزيئة لان عدم وجود تماثل يجعل الحصول على الزوايا والمسافات بين ذرات الجزيئة صعباً.
التماثل في الفيزياء الجزيئية هو التكرار المنتظم في الفضاء لاجسام متشابهة فمثلا جزيئة الهيدروجين تتكون من ذرتي هيدروجين وتفصل بينهما مسافة d فلو قمنا بتدوير احدى الذرتين او الجزيئة كلها حول نقطة تقع في منتصف المسافة d (مركز ثقل الجزيئة) بزاوية 180 فستنطبق الجزيئة على نفسها ونحصل على الترتيب نفسه الذي كانت عليه قبل التدوير وتدعى عملية تدوير الجزيئة حول مركز ثقلها بعملية تماثل symmetry operation.
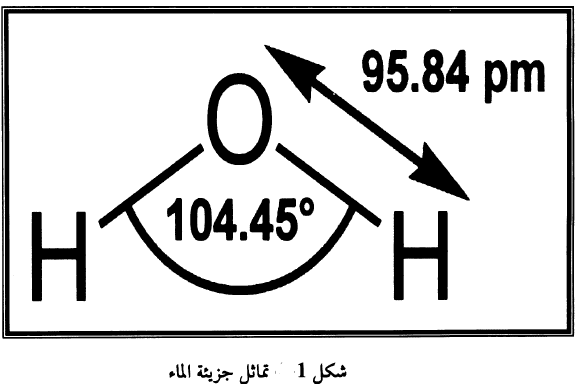
وكذلك فان جزيئة الماء تتكون من ذرة اوكسجين وذرتي هيدروجين وبين ذرتيي الهيدروجين زاويةa كما مبين في شكل 1 والجزيئة متماثلة على جانبي مستوى عمودي في منتصف ذرة الاوكسجين فالجانب الايمن من الجزيئة انعكاس مراة للجانب الايسر ووحدة التماثل لجزيئة الماء ذرة هيدروجين ونصف الاوكسجين وبسبب خاصية التماثل هذه تكفي اعلومتين لوصف جزيئة الماء: مصدار المسافة بين ذرة هيدروجين وذرة الاوكسجين وقيمة الزاوية a بين ذرتي الهيدروجين. طول الآصرة في جزيئة الماء 0.9584 انكستروم وقيمة الزاوية =104.45α
تتم دراسة التماثل في الجزيئات بعناصر التماثل symmetry elements وعمليات التماثل ففي المثال السابق لجزيئة الهيدروجين كان عنصر التماثل محور دوران ولجزيئة الماء كان مستوى انعكاس فمستويات التماثل ومحاور التماثل ونقاط التماثل تدعى جميعا عناصر تماثل ويمكن تصنيف تماثل الجزيئة وفقا لعدد وانواع عناصر التماثل ولهذه الغاية توجد رموز للتعبير عن عناصر التماثل المختلفة.
- محاور التماثل ورمزها Cn للتعبير عن وجود محاور دوران عددها n وتملك الجزيئة محاور تماثل عددها n اذا عادت الى ترتيبها الاولي بعد دوران حول محور بزاوية α= 2π/n وجزيئة الماء تملك محور تماثل C2.
- مستويات التماثل ورمزها σ للتعبير عن وجود مستوى تماثل للجزيئة التي تعود الى ترتيبها الاولي بعد الانعكاس عند هذا المستوى. يدعى المستوى بالمستوى العمودي ويرمز له σv اذا كان محور التماثل للجزيئة Cn يقع على هذا المستوى (اتجاه z)
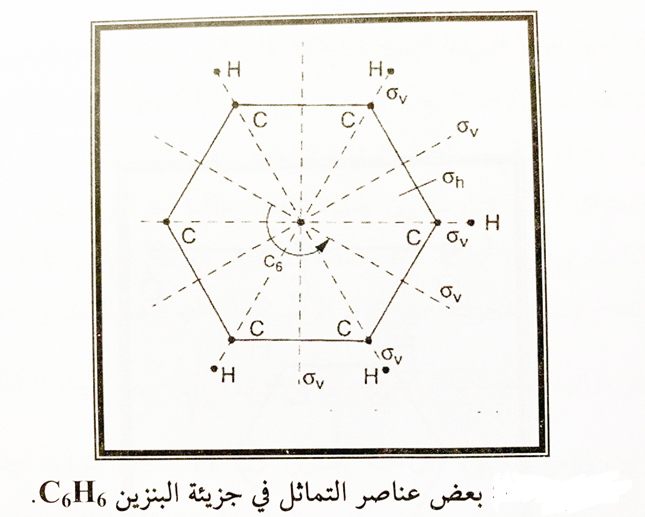
الشكل (2)
نلاحظ ان مستويات التماثل العمودية على هذا المحور (المستوى xy) يرمز لها σh (افقي) وجزيئة الماء تملك مستويين σxy, σv و σxz في شكل 2 بعض مستويات التماثل لجزيئة البنزين C6H6 وفيها ستة مستويات تماثل عمودية σv ومستوى تماثل افقي واحد σh.
- محاور دوران وانعكاس ورمزها Sn للتعبير عن محور تماثل عند دوران الجزيئة بزاوية α= 2π/n حول المحور يتبعها انعكاس عند مستوى عمودي على المحور تعود بعده الجزيئة الى ترتيبها الاولي وجزيئة C3H4 تملك محور تماثل S4 وثلاثة محاور تماثل C2.
- مركز انقلاب ورمزه i للتعبير عن انعكاس كل نواة ذرة في الجزيئة عند هذا المركز. ويقع مركز الانقلاب بالضرورة في مركز ثقل الجزيئة والذي يمثل نقطة الاصل في الاحداثيات المرجعية فكل احداثيات النواة (x.y.z) تتغير اشارتها عند الانقلاب فتصبح (-x,-y,-z) وكل الجزيئات الثنائية الذرة المتشابهة الذرتين مثل جزيئة ثاني اوكسيد الكربون CO2، البنزين C2H2 تملك مركز انقلاب كما مبين في شكل 3. مركز الانقلاب i لجزيئة البنزين C6H6 يقع في مركز الحلقة
السداسية لجزيئة البنزين ومركز الانقلاب i لجزيئة ثاني اوكسيد الكربون CO2 يقع في منتصف ذرة الكربون C.
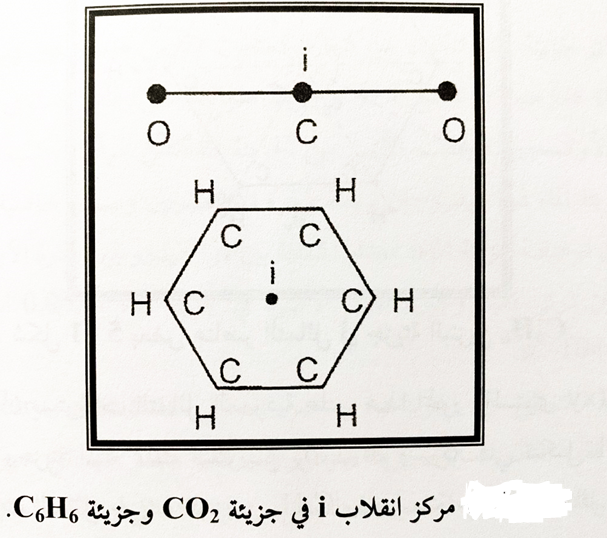
الشكل (3)
ان للتماثل الجزيئي فائدة عظيمة في جمع الانواع الكثيرة جدا من الجزيئات في تصنيفات محدودة وفقا لخواص تماثل الجزيئة، مما يسهل كثيرا تعيين الحالات الجزيئية والانتقالات المسموح بها والانتقالات الممنوعة خلال امتصاص او انبعاث الاشعاع الكهرومغناطيسي خصوصا الجزيئات المتعددة الذرات وقد كان ذلك ممكنا على وجه الخصوص بعد تطبيق نظرية المجموعة لوصف التماثل الجزيئي والتي اعطت تمثيلا دقيقا جدا وواضحا لانواع التماثل الجزيئي.
 الاكثر قراءة في الفيزياء الجزيئية
الاكثر قراءة في الفيزياء الجزيئية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















