
تاريخ الفيزياء

علماء الفيزياء


الفيزياء الكلاسيكية

الميكانيك

الديناميكا الحرارية


الكهربائية والمغناطيسية

الكهربائية

المغناطيسية

الكهرومغناطيسية


علم البصريات

تاريخ علم البصريات

الضوء

مواضيع عامة في علم البصريات

الصوت


الفيزياء الحديثة


النظرية النسبية

النظرية النسبية الخاصة

النظرية النسبية العامة

مواضيع عامة في النظرية النسبية

ميكانيكا الكم

الفيزياء الذرية

الفيزياء الجزيئية


الفيزياء النووية

مواضيع عامة في الفيزياء النووية

النشاط الاشعاعي


فيزياء الحالة الصلبة

الموصلات

أشباه الموصلات

العوازل

مواضيع عامة في الفيزياء الصلبة

فيزياء الجوامد


الليزر

أنواع الليزر

بعض تطبيقات الليزر

مواضيع عامة في الليزر


علم الفلك

تاريخ وعلماء علم الفلك

الثقوب السوداء


المجموعة الشمسية

الشمس

كوكب عطارد

كوكب الزهرة

كوكب الأرض

كوكب المريخ

كوكب المشتري

كوكب زحل

كوكب أورانوس

كوكب نبتون

كوكب بلوتو

القمر

كواكب ومواضيع اخرى

مواضيع عامة في علم الفلك

النجوم

البلازما

الألكترونيات

خواص المادة


الطاقة البديلة

الطاقة الشمسية

مواضيع عامة في الطاقة البديلة

المد والجزر

فيزياء الجسيمات


الفيزياء والعلوم الأخرى

الفيزياء الكيميائية

الفيزياء الرياضية

الفيزياء الحيوية

الفيزياء والفلسفة

الفيزياء العامة


مواضيع عامة في الفيزياء

تجارب فيزيائية

مصطلحات وتعاريف فيزيائية

وحدات القياس الفيزيائية

طرائف الفيزياء

مواضيع اخرى
التركيب الجزيئي Molecular Structure
المؤلف:
الدكتور صلاح الدين محمود يونس
المصدر:
الفيزياء الجزيئية
الجزء والصفحة:
ص 12
23-9-2020
8506
التركيب الجزيئي Molecular Structure
تتوزع الالكترونات في الذرة على مدارات حول النواة وفقا لطاقة الالكترون ومبدأ باولي ويعين المدار بالاعداد الكمية n, 1, m1, ms ويمكن تمثيل المدارات بالدالة الموجية Ψn1 m1 , ms ووفقا لمبدأ باولي لا يمكن لالكترونين لهما نفس قيمة الاعداد الكمية ان يتواجدا في نفس المدار فيكون الترتيب الالكتروني في المدارات وفقا لمقدار الطاقة كما ياتي:
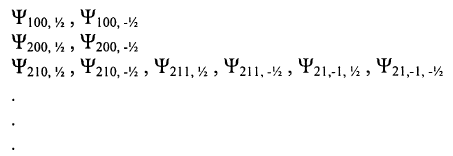
ولكن الحالات التي تملك 1 بقيمة كبيرة معينة من n تنزاح الى طاقات اعلى عند تواجد عدد كبير من الالكترونات مثلا، لذلك تصبح الدوال الموجية السابقة بالشكل:

يشغل الالكترون اقل طاقة ممكن لذلك في ذرة الهيدروجين H الالكترون الوحيد يذهب الى المدار 100,Ψ2/1 او الى المدار 2/1- ,100 Ψ. كل جسيم يجب ان يكون له دالة موجية خاصة به بسبب وجود خاصية البرم الالكتروني electron spin .
حركة الالكترونات في الجزيئات ليست بسيطة كما في الذرات. فالالكترونات في الجزيئة تقفز من ذرة الى ذرة لانها مشتركة بين الذرات وتعود ملكيتها آنيا الى ذرتين او اكثر.
ولكن من الممكن تعيين هذه الحركة بتكوين تراكب خطي Linear combination combination من المدارات الذرية المشغولة بحيث تكون الطاقة الكامنة بأصغر مقدار وكل ذرة من ذرتي الهيدروجين A وB القريبتين من بعضهما وفي الحالة الارضية (أقل طاقة) تملك المدارين:
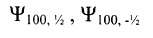
وكل الكترون يستطيع ان يشغل احد المدارين لذلك نحصل على:
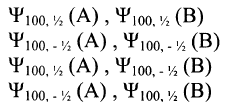
فالحالتان الاولى والثانية حالة تنافر بين الذرتين ولا تشكل جزيئة، بينما الحالتان الثالثة والرابعة حالة تجاذب الذرتين وكل ذرة تشترك بالكترون الذرة الاخرى وتزداد كثافة الشحنة الالكترونية بين النواتين حيث تعمل الشحنة السالبة بين النواتين الموجبتين على ربطهما سوية وتكوين جزيئة.
اما توزيع الكثافة الالكترونية لجزيئة فيمكن توضيحه بافضل صورة باستخدام المنحنيات المغلقة contour map كما موضح في شكل 1 لجزيئة الهيدروجين اذ كل النقاط التي تملك نفس مقدار الكثافة الالكترونية تقع على نفس المنحني المغلق وتقل الكثافة الالكترونية مع الابتعاد عن المحور الذي يربط ذرتي الهيدروجين.
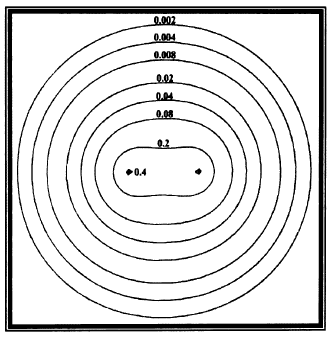
شكل 1: توزيع كثافة الشحنة الالكترونية بين نواتي الهيدروجين
 الاكثر قراءة في الفيزياء الجزيئية
الاكثر قراءة في الفيزياء الجزيئية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















