لما كانت الأمينات ، من الأنواع الثلاثة ، تحتوي على زوج من الالكترونات غير المشتركة ، فإنها ستشبهه بالتأكيد الأمونيا في العديد من الخواص الكيميائية .
وبالذات في ميلهم جميعاً لاستغلال هذا الزوج من الالكترونات غير المشتركة في تكوين روابط جديدة والذي سينتج عنه تفاعلات الأمينات العامة مثل : قاعدتها ، فعاليتها كنيوكليوفيلات وكذلك تأثير هذه الالكترونات في زيادة فعالية الحلقة البنزينية التي يتصل اليها النتروجين كمجموعة معوضية .
قاعدية الأمينات :
تتمكن الأمونيا والأمينات من منح زوج الالكترونات الموجود في المدار المرئي غير المرتبط بذرة النتروجين إلى ذرة أو أيون أو جزيئة فيها نقص أو شحنة في الالكترونات .
ويعدّ الأمين قاعدة ضعيفة في المحلول المائي حيث أنه يكتسب بروتوناً من جزيئة الماء في تفاعل حامض - قاعدة متعاكس وكما بالمعادلة التالية :
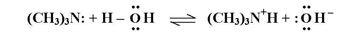
تحويل الأمينات إلى اميدات معوضه :
من المعلوم أن الأمونيا يمكنها التفاعل مع كلوريدات الأحماض العضوية لتنتج الأميدات ، والأميدات كما يعرف الطالب أنها مركبات استبدلت فيها ذرة كلور كلوريد الحامض بمجموعة . - NH2
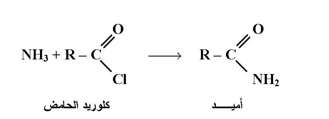
كلك فإنه ليس من الغرب أن بتفاءل كلوريد الامش السلفوني (كلوريد السلفونيل ) مع الأمونيا ينتج سلفوناميد كما بالمعادلة التالية :

وفي هذين التفاعلين استغل تتروجين الأمونيا زوج الاكترونات غير المشتركة ايعمن كعامل نيوكليوفيلي بطرد ذرة الكلور على شكل أيون الكلوريد عند مهاجمته لذرة كأريون الكربونيل . وفي حالة التفاعل مع كلوريد الحامض أو ذرة الكبريت في جزيئة كلوريد السلفونيل .
علما الأمينات الثالثية هي مركبات قاعدية إلا أنها تفشل في تكوين الاميدات أو السلفوناميدات ( تحت ظروف تفاعل هانزنبزج والذي سنشرحه لاحقا ) وذلك بسبب عدم إمكانية فقدانها البروتون بعد اتصالها للكاربون أو الكبريت وكما في المعادلات التالية:
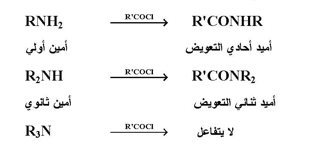
ويمكن استغلال تحضير السلفوناميدات للكشف عن الأمينات المستخدمة في مثل هذه التحضيرات فيما إذا كانت أولية ، ثانوية أو ثالثية معتمدة بذلك على حامضية ذرة الهيدروجين المتصلة على النتروجين في السلفوناميد . ويسمى هذا الكشف بكشف هانزنبرج للأمينات وكما توضح المعادلات التالية :
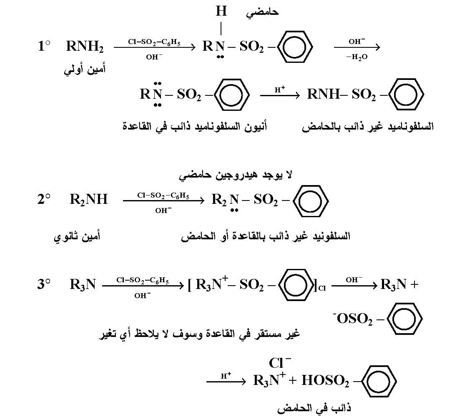
وتسمى الأميدات المعوضة على أساس أنها مشتقة من الأميدات غير المعوضة ، إلا أنه في بعض الحالات الأخرى وبالذات عندما تتضمن الأمينات الاروماتية فإن الأميد يسمى على أساس أنه مشتق من مجموعة الأسيل ، وكما في الأمثلة التالية :
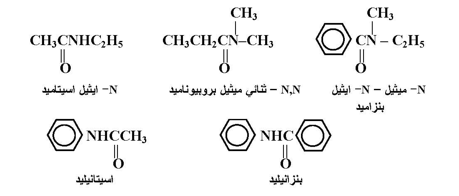
السلفانيل أميد :
يعد أميد حامض السلفونيل ( السلفونيل أميد ) وبعض الأميدات المعوضة الأخرى من المركبات العضوية المهمة بيولوجيا وتسمى بأدوية السلفا . تحضر السلفوناميدات بتأثير كلوريد السلفونيل على الأمونيا اوالأمين .
ويسبب وجود مجموعة أمينو حرة في جزيئة حامض السلفونيك بعض المشاكل التحضيرية فأنه مئلاً إذا رزغب في تحويل حامض السلفانيليك إلى كلوريد الحامض ؛ فأن مجموعة السلفونيل لأحدى الجزيئات ستهاجم مجموعة الأمين الحرة لجزيئة ثنائية لتكوين ارتباط أميدي .
ولقد تم الوصول إلى حل للتغلب على هذه الصعوبة وثلك من خلال وقاية أو حماية مجموعة الأمين باسيلتها فل تحضير كلوريد السلفونيل . وتحضر الملفائيل أميد والمركبات ذات العلاقة بالطريقة التالية :

التفاعل مع حامض النتروز :
لقد وجد أن الأمينات بأنواعها المختلفة ( اليفاتية أو أروماتية ) يمكنها التفاعل مع حامض النتروز : الذي يحضر آنياً من تفاعل حامض الهيدروكلوريك مع نترايت الصوديوم . لتعطي نواتج معتمدة على نوع الأمين المتفاعل . فمثلاً يتفاعل الأنيلين والأمينات الأروماتية الأخرى مع حامض النتروز البارد وفي محلول حامض الهيدروكلوريك لتكون كلوريدات أريل ديازونيوم (ArN2+Cr) أو أملاح الديازونيوم .
وهذه الأملاح فعالة جداً لذلك يجب إجراء التفاعل مع التبريد عند ظروف صفر° م تقريباً ( أملاح الكيل ديازونيوم RN2+Cl وكما سنرى فعالة جداً بحيث أنها تكون غير مستقرة حتى في الظروف الباردة كما يلي :

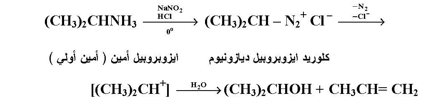
وترجع الفعالية العالية لهذه الأملاح إلى الميل العالي الطرد غاز النتروجين N2 ، لهذا فأنه يمكن استبدال مجموعة الديتزونيوم بنيوكليوفيلات مختلفة مثل I- . كذلك فأن الأمينات الالكيلية الأولية تتفاعل مع نترايت الصوديوم وحامض الهيدروكلوريك لتعطي ملح الديازونيوم الالكيلي .
وهو كما وضحنا من قبل غير مستقر مما سيؤدي إلى تفككه إلى خليط من الكحول والالكيل الناتجين بالإضافة إلى N2 . وتسير عملية التفكك بطريق الكاتيون الكاربوني وكما يلي :
وتتفاعل الأمينات الثانوية ، اليفاتية كانت أم اروماتية مع حامض النتروز لتعطي مركبات N - نتروزو أمينات : مركبات تحتوي على مجموعة –N-N=O. ولقد وجد أن العديد من هذه المركبات هي مركبات مشجعة لتكوين السرطان كما يلي :

ويمكن التعرف على الأمينات من خلال تفاعلها مع حامض النتروز . فلقد وجد أنها تعاني من تفاعل اليكتروفيلي تعويضي على الحلقة لتكون مركبات نتروزو فيها اتصلت مجموعة إلى الكاربون وليس النتروجين .
ويعزى السبب في ذلك إلى ازدياد فعالية الحلقة من خلال مجموعة NR- المنشطة لمثل هذه التفاعلات كما بالمعادلة التالية :
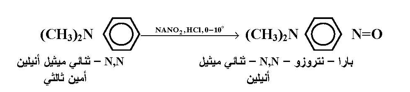
بينما تعاني الأمينات الثالثية الالكيلية من فقدان مجموعة الكيل لتعطي مشتقات N -نتروزو للأمينات الثانوية .
الاستبدال بمجموعة -HO : تحضير الفينولات
إن إحدى الطرق المهمة لتحضير الفينولات معملياً هي من خلال تفاعل أملاح الديازونيوم مع الماء المحمض المغلي ، يحدث التفاعل وبصورة بطيئة في محاليل الديازونيوم المائية الباردة ، لهذا السبب يجب استخدام أملاح الديازونيوم وبصورة مباشرة بعد تحضيرها وذلك تجنباً لتفاعلها مع الماء ، وكما في المعادلة التالية :

الاستبدال بهيدروجين :
يمكن استبدال مجموعة الديازونيوم بهيدروجين بعدد من العوامل المختزلة ، إلا أن العامل الأكثر استخداماً لهذا العرض هو حامض الهايبوفوسفور H3PO2 ؛ حيث تعد هذه الطريق المثلى لحذف مجموعة – NH2 من الحلقة الاروماتية .
وتجرى العملية وبساطة بتوليد أملاح الديازونيوم بوجود حامض الهايبوفوسفور ونتيجة لذلك سيتحرر النتروجين ويتأكسد حامض الهايبوفوسفور إلى حامض الفوسفور H3PO2, وكما يتضح بالمعادلة التالية :

