يشهد الطب الجزيئي في السنوات الأخيرة تطورًا هائلًا في فهم الآليات الكيميائية الدقيقة التي تتحكم بوظائف الخلايا، ومن بين أكثر هذه الآليات أهمية عملية تُعرف باسم Lipidation، وهي ارتباط الدهون بالبروتينات داخل الخلية. لم تعد الدهون تُعرف فقط كمصدر للطاقة أو كمكونات بنيوية للأغشية الخلوية، بل أصبحت تُعد عناصر تنظيمية أساسية تتحكم في توجيه البروتينات وتثبيتها وتنشيطها داخل الخلية. هذا الاكتشاف فتح أبوابًا جديدة أمام العلماء لتطوير أدوية تستهدف الخلايا السرطانية بطريقة دقيقة وأكثر أمانًا من العلاجات التقليدية.
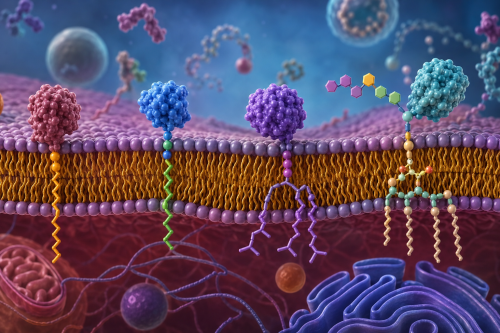
تعتمد العديد من البروتينات الخلوية على ارتباطها بجزيئات دهنية معينة لكي تتمكن من الالتصاق بالغشاء الخلوي وأداء وظائفها الحيوية. وتتم هذه العملية عبر إضافة سلاسل دهنية خاصة إلى البروتينات بواسطة إنزيمات متخصصة داخل الخلية. عندما ترتبط هذه الدهون بالبروتين فإنها تعمل كمرساة جزيئية تُثبت البروتين في الموقع الصحيح داخل الغشاء، مما يسمح له بإرسال واستقبال الإشارات الكيميائية التي تنظم نمو الخلية وانقسامها واستجابتها للمؤثرات الخارجية.
تكمن خطورة هذه العملية في أن بعض الخلايا السرطانية تعتمد اعتمادًا كبيرًا على البروتينات المرتبطة بالدهون لكي تستمر في النمو والانقسام بشكل غير طبيعي. ومن أشهر هذه البروتينات بروتينات RAS التي تُعد من أهم البروتينات المنظمة لنمو الخلية. تحتاج بروتينات RAS إلى الارتباط بالغشاء الخلوي عبر إضافة مجموعة دهنية تُعرف باسم “الفارنيسيل”، وعند حدوث هذا الارتباط تبدأ البروتينات بإرسال إشارات تحفز الانقسام الخلوي المستمر. لكن عندما يتم منع إضافة هذه المجموعة الدهنية يفقد البروتين قدرته على الالتصاق بالغشاء، وبالتالي تتعطل الإشارات الكيميائية التي يعتمد عليها الورم للنمو والبقاء.
انطلاقًا من هذا المبدأ بدأ العلماء بتطوير أدوية حديثة تستهدف عملية ارتباط الدهون بالبروتينات بدل مهاجمة الخلية كاملة كما يحدث في العلاج الكيميائي التقليدي. تعتمد هذه الاستراتيجية على تحديد الإنزيمات المسؤولة عن إضافة الدهون إلى البروتينات، مثل إنزيم Farnesyltransferase، ثم تصميم مركبات دوائية ترتبط بهذا الإنزيم وتمنعه من أداء وظيفته. وبهذا الشكل يتم إيقاف عملية تثبيت البروتين السرطاني على الغشاء الخلوي وتعطيل نشاطه الحيوي.
تمر عملية تطوير هذه الأدوية بعدة مراحل معقدة تبدأ بالدراسات الكيميائية والجزيئية داخل المختبر، حيث يحلل الباحثون التركيب الفراغي للإنزيمات والبروتينات المستهدفة باستخدام تقنيات متقدمة مثل البلورة بالأشعة السينية والمحاكاة الحاسوبية. بعد ذلك تُصمم جزيئات دوائية قادرة على الارتباط بالموقع الفعال للإنزيم ومنع عمله. ثم تُختبر هذه المركبات على الخلايا السرطانية لمعرفة قدرتها على إيقاف الإشارات الجزيئية وتقليل انقسام الخلايا.
وفي المراحل اللاحقة تُجرى تجارب على الحيوانات لدراسة فعالية الدواء وتأثيراته الجانبية، ثم تبدأ التجارب السريرية على البشر للتأكد من أمان العلاج وفعاليته ضد أنواع معينة من السرطان. وقد أظهرت بعض هذه الأدوية نتائج واعدة في تقليل نشاط الأورام وتحسين الاستجابة العلاجية عند المرضى.
كيميائيًا تعمل هذه الأدوية من خلال تعطيل الروابط أو التفاعلات التي تسمح بارتباط السلسلة الدهنية بالبروتين، مما يؤدي إلى فقدان البروتين لموقعه الصحيح داخل الغشاء الخلوي. وعندما يفقد البروتين هذا الموقع تتوقف سلسلة من الإشارات الكيميائية التي تتحكم بالنمو والانقسام والبقاء الخلوي. وتُعد هذه الآلية أكثر دقة من العلاجات التقليدية لأنها تستهدف خطوة جزيئية محددة بدل تدمير الخلايا بشكل عشوائي.
ومع التقدم التكنولوجي الهائل بدأ العلماء باستخدام تقنيات أكثر تطورًا لزيادة كفاءة هذه العلاجات، مثل تقنية النانو تكنولوجي التي تسمح بإيصال الدواء مباشرة إلى الخلايا السرطانية وتقليل تأثيره على الأنسجة السليمة. كما أصبح الذكاء الاصطناعي يُستخدم لتحليل ملايين المركبات الكيميائية وتصميم جزيئات دوائية أكثر دقة وقدرة على استهداف البروتينات المرتبطة بالدهون. إضافة إلى ذلك يجري العمل على تقنيات العلاج الجيني التي تهدف إلى منع تصنيع البروتينات السرطانية أو تعديل الجينات المسؤولة عن عمليات الـ Lipidation داخل الخلية.
إن استهداف ارتباط الدهون بالبروتينات يمثل اليوم أحد أكثر الاتجاهات تطورًا في علاج السرطان والأمراض الجزيئية، لأنه يعتمد على فهم عميق للكيمياء الحيوية داخل الخلية بدل الاعتماد على التدمير العشوائي للخلايا. وهذا المجال لا يفتح الباب فقط لعلاجات أكثر فعالية، بل يمنح الأمل أيضًا في تطوير أدوية ذكية قادرة على مهاجمة الخلايا المريضة بدقة عالية مع تقليل الأضرار الجانبية على الجسم.
































.png) عبد الخالق الفلاح
عبد الخالق الفلاح .png) منذ ساعتين
منذ ساعتين 















 واقعة الغدير.. دلالات وتأملات (1)
واقعة الغدير.. دلالات وتأملات (1) مؤامرة أم "نظرية المؤامرة"
مؤامرة أم "نظرية المؤامرة" إرهاب الميديا
إرهاب الميديا EN
EN