
Benzene and other arenes
 المؤلف:
Peter Atkins, Tina Overton, Jonathan Rourke, Mark Weller, and Fraser Armstrong
المؤلف:
Peter Atkins, Tina Overton, Jonathan Rourke, Mark Weller, and Fraser Armstrong
 المصدر:
Shriver and Atkins Inorganic Chemistry ,5th E
المصدر:
Shriver and Atkins Inorganic Chemistry ,5th E
 الجزء والصفحة:
ص548-549
الجزء والصفحة:
ص548-549
 2025-10-01
2025-10-01
 627
627
Benzene and other arenes
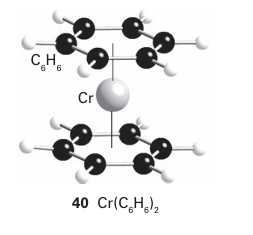
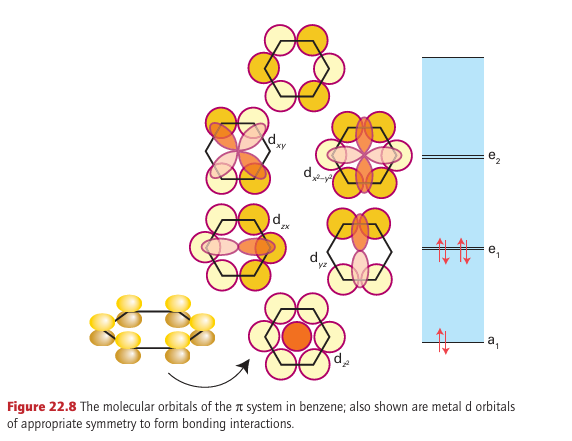
Key point: A consideration of the MOs of benzene leads to a picture of bonding of benzene to a metal atom that includes a significant δ back bonding interaction. If benzene is considered to have three localized double bonds, each double bond can behave as a ligand and the molecule could behave as a tridentate η6-ligand. A compound such as bis(η6-benzene) chromium (40) could then be considered to be made up of six coordinated double bonds, each donating two electrons, bound to a d6 metal atom, giving a total of 18 valence electrons for the octahedral complex. Bis(η6-benzene) chromium does exist, and is remarkably stable: it can be handled in air and sublimes with no decomposition. Although this description of the bonding is a first step towards understanding its structure, the true picture needs a deeper consideration of the molecular orbitals involved. In the molecular orbital picture of the π bonding in benzene there are three bonding and three antibonding orbitals. If we consider a single benzene molecule bonding to a single metal, and consider only the d orbitals, the strongest interaction is a σ interaction between the most strongly bonding a1 benzene MO and the dz2 orbital of the metal atom; π bonds are possible between the two other bonding benzene MOs and the dzx and dyz orbitals. Back bonding from the metal atom to the benzene is possible as a δ interaction between the dx2-y2 and dxy orbitals and the empty antibonding e2 orbitals of benzene (Fig. 22.8). η6-Arenes are considered to be neutral ligands that donate six electrons and are normally considered to take up three coordination sites at a metal.
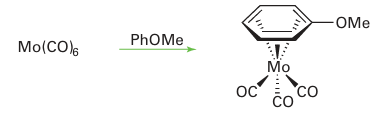
Hexahapto (η6) arene complexes are very easy to make, often simply by dissolving a compound that has three replaceable ligands in the arene and refluxing the solution:
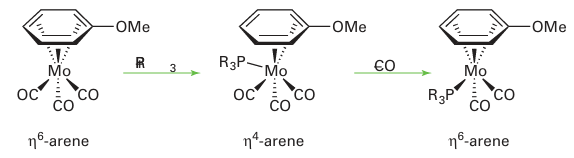
One commonly invoked reaction intermediate of η6-arene complexes is a ‘slipping’ to an η4 complex, which donates only four electrons to the metal, and therefore allows a substitution reaction to proceed without an initial ligand loss:
η2-Arenes are also known and are analogous to η2-alkenes; they have an important role in the activation of arenes by metal complexes.
 0
0
 0
0
لا توجد تعليقات بعد
ما رأيك بالمقال : كن أول من يعلق على هذا المحتوى
 الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة
