

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
Carbides
المؤلف:
CATHERINE E. HOUSECROFT AND ALAN G. SHARPE
المصدر:
Inorganic Chemistry
الجزء والصفحة:
p 357
6-2-2018
2488
Carbides
Classifying carbides is not simple, but some useful categories are:
- saline (salt-like) carbides which produce mainly CH4 when hydrolysed;
- those containing the [C≡C]2- ion;
- those containing the [C=C=C]4- ion;
- interstitial carbides;
- solid state carbides with other lattice structures;
- fulleride salts
- endohedral metallofullerenes
Examples of saline carbides are Be2C and Al4C3, both made by heating the constituent elements at high temperatures. Although their solid state structures contain isolated C centres which are converted to CH4 on reaction with H2O, it is unlikely that the ‘C4-’ ion is present since the interelectronic repulsionenergy would be enormous. Carbides containing the [C≡C]2- (acetylide) ion include Na2C2, K2C2, MC2 (M=Mg, Ca, Sr, Ba), Ag2C2 and Cu2C2; they evolve C2H2 when treated with water. Calcium carbide is manufactured as a grey solid by heating CaO with coke at ≈ 2300 K, and when pure, it is colourless. It adopts a distorted NaCl lattice, the axis along which the [C≡C]2- are aligned being lengthened; the C_C bond distance is 119 pm, compared with 120pm in C2H2. The reaction between CaC2 and N2 is used commercially for the production of calcium cyanamide, a nitrogenous fertilizer. The cyanamide ion is iso electronic with CO2.
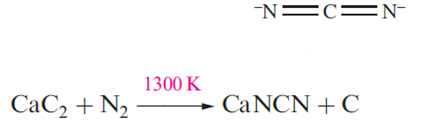

Equations 13.30 and 13.31 show syntheses of Na2C2, Ag2C2 and Cu2C2; the group 11 carbides are heat- and shock-sensitive, and explosive when dry.
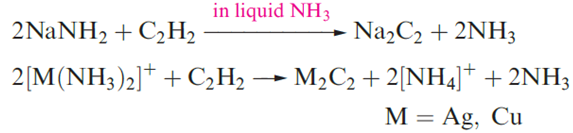
Carbides of formula MC2 do not necessarily contain the acetylide ion. The room temperature form of ThC2 (Th is an actinoid metal, see Chapter 24) adopts an NaCl lattice but is not isostructural with CaC2. In ThC2 , the C2 –units (dCC = 133 pm) in alternating layers lie in different orientations.The solid state structure of LaC2 contains C2-units with dCC = 129 pm. Unlike CaC2 which is an insulator, ThC2 and LaC2 have metallic appearances and are electrical conductors. The C_C bond lengths can be rationalized in terms of structures approximating to Th4[C2]4- and La3[C2]3-; compared with [C2]2-, the extra electrons in [C2]4- and [C2]3- reside in antibonding MOs, thus weakening the C_C interaction. However, the conducting properties and diamagnetism of ThC2 and LaC2 show that this is an oversimplified description since electron delocalization into a conduction band (see Section 5.8) must occur. Hydrolysis of these carbides is also atypical of a [C2]2--containing species, e.g. the reaction of ThC2 and H2O yields mainly C2H2, C2H6 and H2. Carbides containing [C=C=C]4- are rare; they include Mg2C3 which liberates propyne upon hydrolysis. The structures of the so-called interstitial carbides (formed by heating C with d-block metals having rmetal > 130 pm, e.g. Ti, Zr, V, Mo, W) may be described in terms of a closepacked metal lattice with C atoms occupying octahedral holes.
In carbides of type M2C (e.g. V2C, Nb2C) the metal atoms are in an hcp lattice and half of the octahedral sites are occupied; in the MC type (e.g. TiC and WC), the metal atoms adopt a ccp structure and all the octahedral holes are occupied. These interstitial carbides are important refractory materials; characteristically they are very hard and infusible, have melting points >2800K and, in contrast to the acetylide derivatives, do not react with water. Tungsten carbide, WC, is one of the hardest substances known and is widely used in cutting tools and dies. Although TiC, WC, V2C, Nb2C and related compounds are commonly described as interstitial compounds, this does not imply weak bonding. To convert solid carbon into isolated carbon atoms is a very endothermic process and this must be compensated by the formation of strong W_C bonds. Similar considerations apply to interstitial nitrides . Transition metals with rmetal < 130 pm (e.g. Cr, Fe, Co, Ni) form carbides with a range of stoichiometries (e.g. Cr3C2, Fe3C) which possess complicated structures involving C_C bonding. In Cr3C2 (formed by reaction 13.32), the Cr atoms form a lattice of edge-sharing trigonal prisms each occupied by a C atomsuch that carbon chains run through the structure with C_C distances comparable to single bonds.

Carbides of this type are hydrolysed by water or dilute acid to give mixtures of hydrocarbons and H2.
 الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















