

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الإضافة الالكتروفيلية : التوجيه والتفاعلية
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 358
1-4-2017
13267
الإضافة الالكتروفيلية : التوجيه والتفاعلية
Electrophilic addition : orientation and reactivity
تكون الآلية متوافقة مع (د) توجيه إضافة الكواشف الحمضية و (هـ) تأثير البنية في التفاعلية النسبية للألكنات.
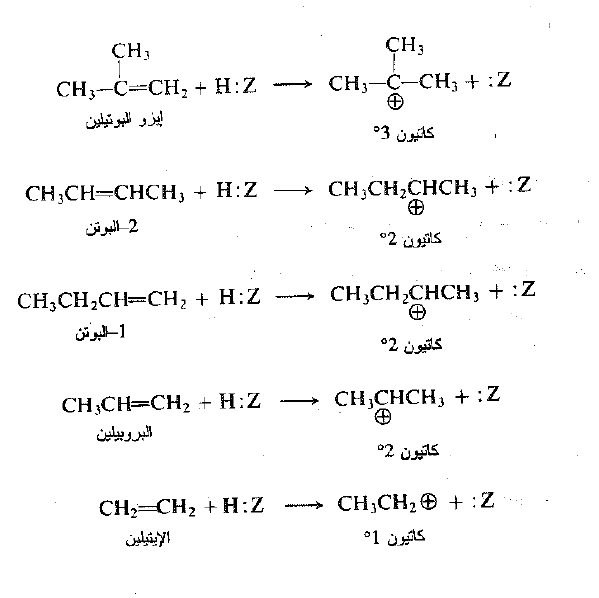
نوجز أدناه إضافة كلوريد الهيدروجين إلى ثلاثة الكنات نموذجية مع خطوتي الآلية المعطاة. بالانسجام مع قاعدة ماركوفنيكوف، يعطي كلوريد ايزو البروبيل، ويعطي ايزو البوتيلين كلوريد ثالثي البوتيل، ويعطي -2 متيل -2- البوتن كلوريد ثالثي البنتيل.
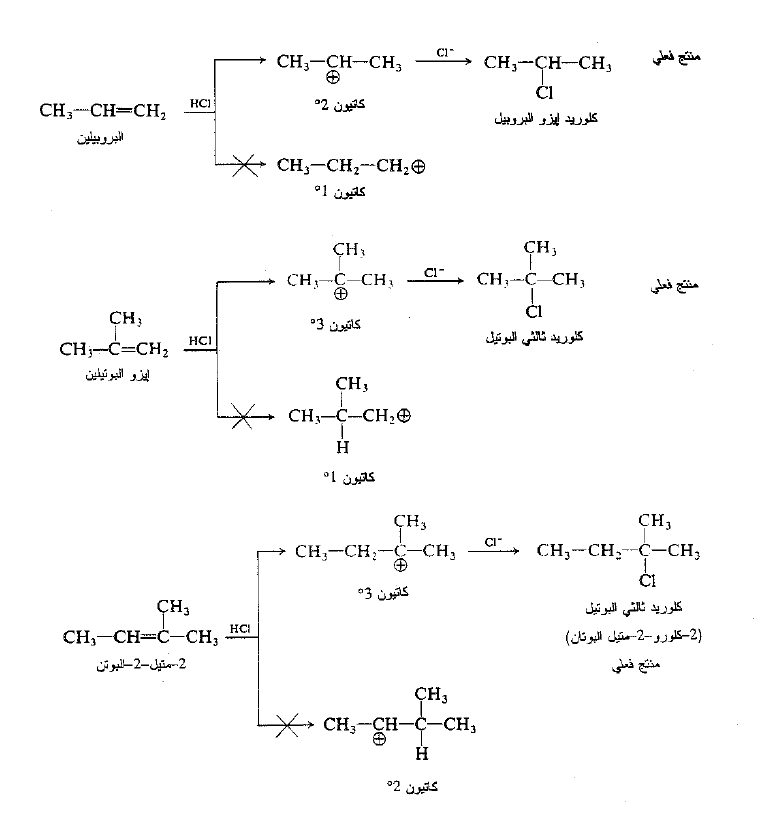
ووفقاً للآلية ، يضاف الهيدروجين المأخوذ من الكاشف إلى إحدى ذرتي كربون الرابطة المزدوجة او إلى الأخرى ليعطي أحد الكربوكاتيونين المحتملين او الكربوكاتيون الآخر. فمثلاً ، إذا ذهب الهيدروجين إلى C – 2 في البروبيلن، يتشكل الكاتيون نظامي البروبيل، وإذا ذهب إلى C – 1 ، يتشكل الكاتيون ايزو البروبيل. وحال تشكلهما يتفاعل الكربوكاتيون بسرعة ليعطي المنتج. يعتمد نوع الهاليد الذي نحصل عليه عندئذ على الكربوكاتيون المتشكل في الخطوة الاولى . إن حقيقة ان البروبيلين يعطي كلوريد ايزو البروبيل عوضاً عن كلوريد نظامي البروبيل تظهر ان كاتيون ايزو البروبيل يتشكل بدلاً من (أي أسرع) الكاتيون نظامي البروبيل. لذلك ، تحدد التوجيه في الإضافة الالكتروفيلية بالسرعتين النسبيتين للتفاعلين المتنافسين. تشكل الكربوكاتيون الأول أو الآخر.
في كل الأمثلة، المعطاة أعلاه : يظهر المنتج الحاصل انه في الخطوة الابتدائية يتشكل كاتيون ثانوي بأسرع من الكاتيون الأولى، او الثالثي بأسرع من الأولى، أو الثالثي بأسرع من الثانوي. يظهر فحص التوجيه في حالات كثيرة هذا الأمر قاعدة عامة، اي في الإضافة الالكتروفيلية تتبع سرعة تشكل الكربوكاتيونات التسلسل التالي:
سرعة تشكل الكربوكاتيونات 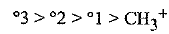
عند ترتيب الكربوكاتيونات حسب سرعة تشكلها من الالكنات ، غير اننا نجد ثانية، رتبناها حسب تسلسل الاستقرار:
استقرار الكربوكاتيونات 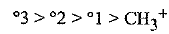
يمكننا اعادة صياغة ماركوفنيكوف كالتالي: يتضمن تفاعل الإضافة الالكتروفيلية إلى الرابطة المزدوجة كربون – كربون تشكل مركبات متوسطة من الكربوكاتيونات الاكثر استقراراً.
كما في قاعدة زايتسف فإن إعادة الصياغة هذه تعطي قاعدة تكمن اهميتها ليس في تطبيقاتها الاكثر استخداماً، وانما في ايصالنا إلى العامل الفاعل في الواقع.
كيف يمكننا تفسير حقيقة ان سرعة تشكل الكربوكاتيون في الإضافة الالكتروفيلية ، تعتمد على استقراره ؟ مرة اخرى يجب ان نقارن بنية المتفاعلات مع بنية الحالة الانتقالية. يرتبط الهيدروجين إلى Z:، ويرتبط كربوناً الرابطة المزدوجة إلى بعضهما ليس فقط بالرابطة σ ولكن أيضاً بالرابطة π بينما في المنتجات، يرتبط الهيدروجين إلى احد الكربونين، وتكون الرابطة بين الهيدروجين و Z: جزئياً، وتتشكل الرابطة بين الهيدروجين والكربون ، وتكون الرابطة π مكسورة جزئياً ويكتسب الكربون جزئياً شحنة موجبة سوف يحملها في الكربوكاتيون.
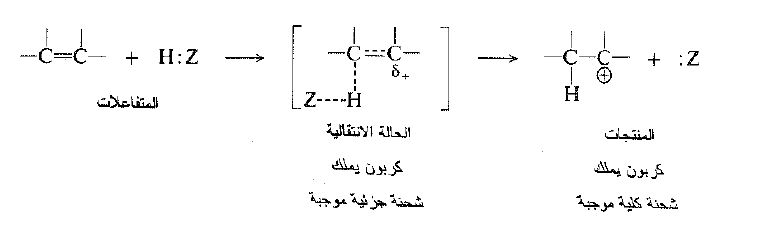
تميل الزمر المانحة للألكترونات إلى تشتيت الشحنة الجزئية المتشكلة على الكربون، وبهذه الطريقة نستقر الحالة الانتقالية. يخفض استقرار الحالة الانتقالية من Eact ويسمح بتفاعل اسرع (انظر الشكل 1.1). وتمتلك الزمر العضوية سمات الكربوكاتيون الذي يتشكل حسب مدى الكسر الذي تعاني منه الرابطة π وكما في السابق، فإن نفس العامل، وهو عامل تحرر الالكترونات ، يجعل الكربوكاتيون مستقراً يؤدي ايضاً إلى استقرار الكربوكاتيون الابتدائية في الحالة الانتقالية.
ونجد ثانية ان الكربوكاتيون الاكثر استقراراً هو الاسرع تشكلاً.
لذلك، تعتمد سرعة إضافة ايون الهيدورجين إلى الرابطة المزدوجة على استقرار الكربوكاتيون المتشكل. وكما نتوقع، فإن هذا العامل لا يحدد فقط توجيه الإضافة إلى الكن معين، ولكن ايضاً التفاعليات النسبية لألكنات مختلفة.
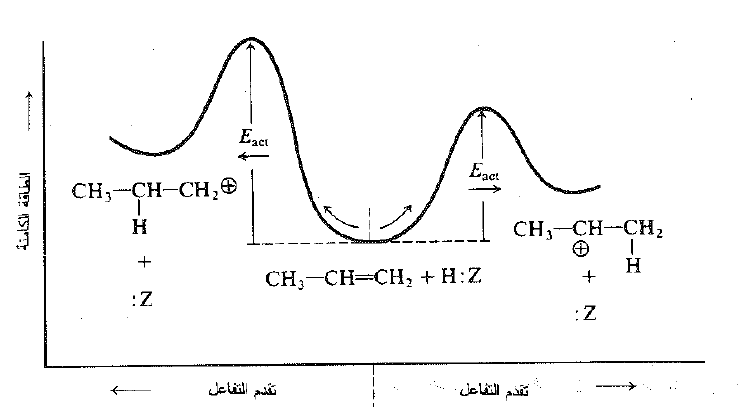
الشكل 1.1 البني الجزيئية وتوجيه التفاعل. يتوازى استقرار الحالة الانتقالية مع استقرار الكربوكاتيون. الكربواكتيون الاكثر استقراراً هو الاسرع تشكلاً.
تظهر الالكنات عادة الترتيب التالي للتفاعلية تجاه إضافة الحموض:
تفاعلية الالكنات تجاه الحموض
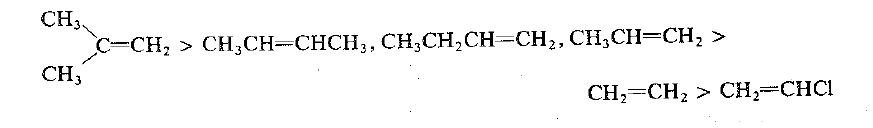 يتفاعل ايزو البوتيلين الذي يشكل كاتيوناً ثالثياً بشكل اسرع من -2 البوتن الذي يشكل كاتيوناً ثانوياً. ويتفاعل -1 البوتن ، -2 البوتن والبروبيلين والذين يشكلون كاتيونات ثانوية بشكل اسرع من الايتيلين الذي يشكل كاتيوناً اولياً.
يتفاعل ايزو البوتيلين الذي يشكل كاتيوناً ثالثياً بشكل اسرع من -2 البوتن الذي يشكل كاتيوناً ثانوياً. ويتفاعل -1 البوتن ، -2 البوتن والبروبيلين والذين يشكلون كاتيونات ثانوية بشكل اسرع من الايتيلين الذي يشكل كاتيوناً اولياً.
تميل الهالوجينات ، بوصفها متبادلات ، إلى جذب الالكترونات . كما يؤدي تحرير زمر الالكيل للالكترونات إلى تشتيت الشحنة الموجبة واستقرار الكربوكاتيون. كذلك، فإن سحب الالكترونات من قبل الهالوجينات يؤدي إلى زيادة شدة الشحنة الموجبة وإلى عدم استقرار الكربوكاتيون. ونلاحظ أن هذا السحب الالكتروني يبطئ من تشكل الكربوكاتيونات في التحلل اللامتجانس . وينفس الطريقة يبطئ من تشكل الكربوكاتيونات في الإضافة الالكتروفيلية. فمثلاً ، يكون كلوريد الفينيل CH2 = CHCl اقل تفاعلية من الايتيلين.
عندما قلنا ان الكربوكاتيون هو صميم آلية الإضافة الالكتروفيلية ، لم نقصد فقط بأنه مركب متوسط، ولكن قصدنا انه كما في تفاعلات الكربوكاتيونات الاخرى التي درسناها ، تكون سرعة تشكل الكربوكاتيون هي التي تعين مسار التفاعل.
نستطيع ان نبدأ برؤية قوة السلاح الذي تمتلك لمواجهة المشكلة التي تنشأ عندما يتعلق الأمر بعدد متنوع من التفاعلات التي تشتمل على الكربوكاتيونات. نحن نعلم، انه كلما كان الكربوكاتيون اكثر استقراراً كان تشكله اسرع، ويعتمد استقراره على تشتت الشحنة، وبتعين تشتت الشحنة هذا بالتأثير الالكتروني للزمر المرتبطة. لقد وجدنا سابقاً ان نفس الامر جعلنا قادرين على التعامل مع مسائل مختلفة، مثل (أ) التفاعليات الركائز في الاستبدال SN1، (ب) السهولة النسبية في نزع الماء من الكحولات ، (جـ) التفاعليات النسبية للألكنات عند إضافة الحموض ، (د) توجيه إضافة الحموض إلى الالكانات ، و (هـ) طراز إعادات الترتيب التي يمكن ان تحدث في جميع هذه التفاعلات .
 الاكثر قراءة في الهايدروكاربونات
الاكثر قراءة في الهايدروكاربونات
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















