
تقليل المقاومة للمضادات الحيوية والتوجهات الحديثة
 المؤلف:
زهرة محمود الخفاجي
المؤلف:
زهرة محمود الخفاجي
 المصدر:
التقنية الحيوية الميكروبية
المصدر:
التقنية الحيوية الميكروبية
 الجزء والصفحة:
الجزء والصفحة:
 20-9-2016
20-9-2016
 1375
1375
تقليل المقاومة للمضادات الحيوية والتوجهات الحديثة
بعد انقضاء أكثر من نصف قرن على طرح واستعمال المضادات الحيوية لا زالت الامراض الناتجة عن الاصابات تشكل نصف الامراض المؤدية للوفيات، وقد زادت المقاومة في معظم السلالات المرضية اذ اصبحت بعض الاصابات لا يتوفر لها علاج ولعل اخطرها ظهور سلالات خاصة من بكتريا السل المقاومة والتي ظهرت عالميا مرافقة لمرض نقص المناعة المكتسبة AIDS ، وهناك بعض المحاولات التي اتخذت للتغلب على هذه المشكلة التي تتفاقم باستمرار، ومن هذه المحاولات :
- استعمال تراكيز عالية من المضادات لزيادة تركيزها في الانسجة المصابة ولمنع الاحياء من تطوير المقاومة.
- استعمال أكثر من دواء او مضاد سوية على ان تكون مختلفة الاهداف وكذلك مختلفة البنية التركيبية للابتعاد عن ظهور المقاومة المتداخلة.
- اجتناب تعريض الاحياء للتراكيز الواطئة من الأدوية لتفادي تدريبها على المقاومة.
- تجفيف الموارد المؤدية لظهور المقاومة مثل عدم استعمال المضادات الحيوية في أعلاف الحيوانات والمواد الحافظة للأغذية.
- التقليل الى أبعد حد ممكن من استعمال المضادات ذات المدى الواسع من التأثير.
ونظرا لكون استعمال المضادات من الطرق الملائمة للعلاج لان العلاج بها يعد قصير الأمد، ومن جهة ثانية فان كل دواء يحتاج الى حوالي 8 – 10 سنوات (عند استعمال المسح العشوائي) من حين الاكتشاف الى الاستعمال واطلاقه الى السوق، اذ يحتاج الى العديد من الخطوات ومراحل سريرية متعددة، ثم الخضوع للعديد من عمليات التقييم وعبور التقييدات والتشريعات مما حدى بالعاملين بالقفز على هذه الحواجز باستعمال المضادات المجازة اصلا واجراء التحوير عليها املا في التخلص من المقاومة، ولذلك بدأت تظهر الأدوية على شكل أجيال وأجيال من المضادات ومن أهم (واحد الأمثلة من العديد) اجيال المضادات الحيوية السيفالوسبورينات الموضحة في الشكل (1). ولكن معظم هذه المحاولات باءت بالفشل. وأصبحت عملية انتاج مضادات جديدة عملية خسارة اقتصادية وخسارة في مواجهة الاحياء المجهرية الممرضة وأدت الى انسحاب الصناعات الصيدلانية من تطوير مضادات للميكروبات، وهذه تعد مشكلة جماعية وتؤثر على الصحة العامة. ويمكن ملاحظة ذلك من قلة عدد المضادات الجديدة المسجلة فمثلا بين عامي 1998 – 2002 تراجعات النسبة بـ 56% بالنسبة لشركات الادوية الكبرى العالمية عما كانت عليه بين عامي 1983 – 1987 ، اما في عام 2002 لم يسجل اي طلب لتسجيل للمضادات الجديدة ويمكن ملاحظة ذلك من الشكل (2).
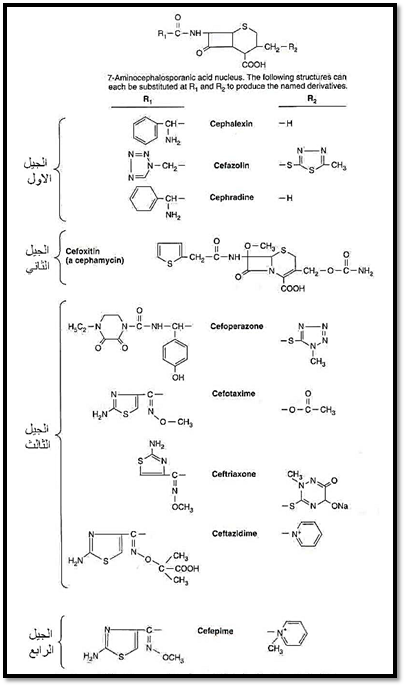
شكل 1 : الاجيال المختلفة من السيفالوسبورينات لتلافي مقاومة الاحياء المجهرية
وهذه الحالة أدت الى الشعور بالقليل من قبل الجهات المختصة لذلك زادت هذه المؤسسات مثل FDA و WHO من اهتمامها وبدأت بتشجيع الصناعات الصيدلانية بالعودة الى البحث والتقصي عن الادوية المضادة للميكروبات المرضية وذلك بإقامة المؤتمرات ورصد الموارد المالية الكبيرة لتصب في هذا الاتجاه.
إذن المقاومة في الاحياء المجهرية هي المحفزة للبحث عن وسائل جديدة لاستهداف الآليات غير المستغلة مسبقا لتأثير المضادات. وبدأت الجهود الجادة التي يمكن وضع بعضها في النقاط الآتية :
- التركيز على دراسة الكيمياء التركيبية للمضادات الموجودة أصلا والمركبات الجديدة.
- دراسة الاهداف الممكن استهدافها.
- تطوير عمليات المسح السريعة مثل High throughput screens التي تساعد بمسح الآلاف من المواد بوقت قصير جدا.
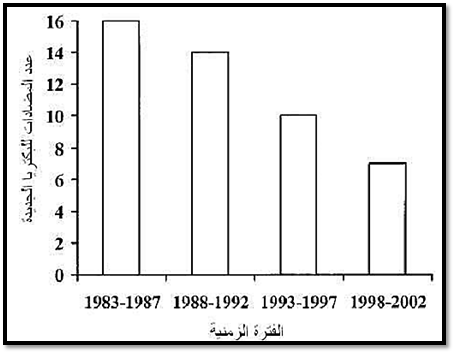
شكل 2 : مستويات تصنيع واكتشاف المضادات الحيوية الجديدة
ولا تزال الاهداف في الخلايا البكتيرية هي التقليدية الممكن استهدافها مثل المواد النووية والجدران والاغشية الخلوية، والجديد في الوقت الحاضر استغلال المسارات والعوامل التي تشارك فيها والتي اسفرت الدراسات الجزيئية في الكشف عنها، ومن أهم الاهداف هي المضخات التي تضخ المضادات الى خارج الخلايا المقاومة، وكذلك استهداف عمليات تخليق الحوامض الدهنية ومزامرتها تحت ظروف الاجهاد. كما ان الدراسات تستهدف الخلايا الهاجعة التي تمثل عقبة كبيرة لأنها الاكثر مقاومة وكذلك الخلايا بطيئة النمو. وتستهدف الدراسات معرفة فسلجه الخلايا تحت ظروف الاجهاد ومعرفة كيفية تصرف الخلايا عند استعمال ممهدات الاجهاد خاصة بوجود المضادات التي تمثل احد الاجهادات على الخلايا. ودراسة مسارات نقل الاشارات والاستجابات الناتجة، وكذلك تكثيف الدراسات على الاحياء التي تتطفل داخل الخلايا والتي من المفارقات ان بعضها تتطفل داخل اجهزة دفاعات الجسم وهو الجهاز المناعي.
واجراء الدراسات حول الاحياء الموجودة داخل الأغشية الحيوية التي تمثل العقبة الكوؤد امام استعمال المضادات الحيوية ومقارنة نمط حياة الخلايا بشكل هائم او عالق مع نمط الحياة في الأغشية الحيوية. وتعتمد الجهات البحثية على ما توصلت إليه العلوم الجزيئية في الاحياء المجهرية. فقد تم تحديد توالي جينومات بعض البكتريا مثل H. influenza (عام 1995) وتلت ذلك العديد من الاحياء خاصة ذات العلاقة بالحالات المرضية السريرية والتي وفرت معلومات جينومية قيمة عن الجينومات ساعدت في فهم جوانب كبيرة من فسلجه الخلايا.
وتتم الاستعانة بقواعد معلوماتية حول المكنون البروتيني للبكتريا Bacterial proteome وكذلك مكنون النسخ Transcriptome لتحديد عوامل الانتساخ ومواقع ارتباطها لاستعمالها كأهداف. كل هذه تساعد في تحديد طريقة التأثير (Mechanism of action) MOA التي تساعد في التكهن لعمل المركبات مما يهيئا الفرصة لإيجاد نسق تعبيري لطرق التأثير البديلة باستعمال الطفرات او ايجاد مضادات تعمل على أهداف جديدة. ومما يؤثر في فعالية توجيه طرق التأثير هو توفر القواعد المعلوماتية كي تكون مراجع يقاس عليها.
وقد أسفرت المحاولات عن بعض الجوانب المشجعة ومنها :
- القيام بتطوير برامج لدراسة وانتاج الأدوية اليتيمة Orphan drugs وهي التي تنتج بكميات قليلة لان الحاجة إليها قليلة وبذلك فهي غير مجدية من الناحية الاقتصادية ولكن المحاولات ترمي الى توسيع مجالات استخدامها، حتى ان بقيت بمستوى خسارة اقتصادية فان الشركات يمكن ان تعوض من مبيعات اخرى او من المنح المالية التي تقدمها الجهات المختصة.
- انتاج المضادات الهجينة، اذ يهدف التوجه الى تخليق مضاد حيوي مكون من قطعتين من المضادات وذلك بهندسة الاحياء المنتجة وإدخال الجينات الخاصة بتخليق الانزيمات من كائنين مختلفة منتجة لمضادات مختلفة وانتاج مضاد حيوي واحد. وقد تمت الاستفادة من Streptomyces المهندس وراثيا لإنتاج مضادات جديدة من مجموعة Macrolides.
- محاولة الاستفادة من الاحياء غير المستغلة مثل الاحياء البحرية والطحالب لان الاعتقاد (ومن ورائه اليقين) ان الاحياء تنتج عددا هائلا من المركبات التي لبعضها صفات مضادة للميكروبات.
- التوجه الى دراسة المضادات المنتجة من المملكة الحيوانية فالعديد من الحيوانات وخاصة اللافقريات التي لا تمتلك جهاز مناعي كفؤ.
فالحيوانات تنتج عددا من المضادات وأغلبها من البروتينات أو البيبتيدات من خلايا الجهاز المناعي تقوم بنخر الخلايا المصابة بالفيروسات او غيرها من الممرضات، ومن أمثلتها Defesin البروتين الذي يؤدي الى زيادة نضوحيه الأغشية الخلوية للبكتيرية، وهناك مركبات اخرى مشابه في التأثير مثل Bactenecin , Azurodicin و Lsozyme الذي يحلل جدران البكتريا الموجبة لصبغة كرام بشكل خاص، وكذلك البروتين Lactoferrin الذي يمنع نمو البكتريا بحسب ايونات الحديد الحرة بقوة.
- استهداف الامراضية وعوامل الضراوة Pathogenesis – targeted antibiotics ويهدف التوجه دراسة عوامل الضراوة التي تؤدي الى توليد الامراض والظروف المشجعة لها مثل ظروف الاجهاد واستهدافها بدلا من القضاء على الخلايا كاملة وبذلك يمكن القضاء على البكتريا المقاومة، وفي هذه الحالة ستكون المضادات المستعملة مختلفة عن المضادات التقليدية ومن ثم لا تنشأ المقاومة. كما انها لا تشكل ضغطا انتخابياً يؤدي في النهاية الى تطور المقاومة اذ سيكون مؤثرا على الاحياء الممرضة فقط. وتستهدف مشاريع دراسة تواليات الجينومات التعرف على المناطق المسئولة عن الامراض وعوامل الضراوة.
- استعمال العاثيات لعلاج الاصابات البكتيرية وهي طرق ليست تقليدية، فالعاثيات تستعمل في بحوث الوراثة والتعرف على الاهداف الخاصة من بروتينات الارتباط، كما انها تستعمل وسيلة لإيصال اللقاحات الوقائية. وقد اجريت التجارب لاستعمال العاثيات الخيطية كحامل للأدوية للتخلص من البكتريا المرضية، وحور العاثي لإيجاد جزء استهداف على سطحه يستخدم لربط الدواء على السطح بوصلة غير ثابتة Labile linker لغرض إطلاق الدواء عند الحاجة. فعندما يكون الدواء مرتبطا الى العاثي فانه يكون بمثابة دواء أولي Prodrugs ويكون غير فعال فيخلو من القابلية السمية للخلايا ولكنه ينشط بعد اطلاقه من العاثي عند موقع الهدف. كما ان هناك محاولات لاستعمال العاثيات الخاصة ببكتريا السل Mycophages لغرض معالجة السلالات التي ظهرت مع اجتياح موجة الايدز والاخرى التي تظهر مقاومة لعدد من المضادات والأدوية قيد الاستعمال، ومثل هذا التوجه يفيد لبعض المضادات التي تكون فعالة ضد البكتريا الممرضة ولكنها لا تستعمل لتأثيراتها الجانبية على المضيف مثل الكلورومفينكول وكذلك مع الادوية ذات السمية الانتقائية الواطئة لمواجهة المقاومة.
ولابد ان تكون هناك أفكار وأفكار يمكن ان تنشا للحاجة الملحة للبحث عن الأدوية الجديدة ما دام الإنسان في صراع مع الاحياء الاخرى.
المصادر
الخفاجي , زهرة محمود (2008) . التقنية الحيوية الميكروبية (توجهات جزيئية ) . معهد الهندسة الوراثية والتقنية الحيوية . جامعة بغداد .
 الاكثر قراءة في التقنية الحيوية والطب
الاكثر قراءة في التقنية الحيوية والطب
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة
